什么是無菌
無菌是指在產(chǎn)品上不存在任何存活的微生物的狀態(tài)。滅菌就是殺滅細菌及其細菌繁殖體、芽孢、病毒和真菌孢子等一切形式的微生物的過程。
大量研究證明,物理和化學因子對于微生物的殺滅遵循指數(shù)法則。隨著滅菌作用時間的延長,產(chǎn)品上的微生物數(shù)量級近似于線性的下降。但是,任何產(chǎn)品經(jīng)過任何滅菌過程,其攜帶的微生物始終有一定的存活概率。可以這樣說,沒有一種滅菌方法可以**保證無菌,而只能將存活概率降低到極低水平。《ISO 11135 醫(yī)療器械環(huán)氧乙烷滅菌的確認和常規(guī)控制》規(guī)定了無菌醫(yī)療器械的帶菌概率需在10 -6 cfu以下,該概率被稱為為無菌保證水平(Sterile Assurance Level ,SAL)。
環(huán)氧乙烷滅菌
環(huán)氧乙烷作為一種廣譜低溫滅菌劑,目前在世界各G廣泛的應(yīng)用于醫(yī)院和工業(yè)*域。據(jù)統(tǒng)計,有50%以上的生產(chǎn)廠商選用環(huán)氧乙烷對其醫(yī)療器械產(chǎn)品進行滅菌。
環(huán)氧乙烷又稱作氧化乙烯,分子式為C 2 H 4 O,分子量為44.05,在常溫常壓下為氣態(tài),具有很強的化學活性和穿透性,可以穿過微孔,到達產(chǎn)品深層,從而大大提高了滅菌效果。
影響環(huán)氧乙烷滅菌效果的因素通常包括溫度、相對濕度、環(huán)氧乙烷濃度和時間。
在一定范圍內(nèi),溫度升高導致氣體分子活動加劇,從而提高了環(huán)氧乙烷的滅菌效率。然而,在超過一定溫度以后,滅菌效率的上升不明顯。而且, 過高的溫度也可能對產(chǎn)品造成損害。因此,通常選用的滅菌溫度為40℃~60℃。
水是烷基化反應(yīng)的反應(yīng)劑,能打開環(huán)氧乙烷的環(huán)氧基團以使烷基化反應(yīng)能順利進行。另外,水能夠加速環(huán)氧乙烷的穿透,提高滅菌效率。研究證明,濕度對于環(huán)氧乙烷滅菌成功起著非常關(guān)鍵的作用。比較理想的濕度范圍是40%~80%,如濕度低于30%,容易導致滅菌失敗。
在一定溫度和濕度條件下,環(huán)氧乙烷的濃度升高可使滅菌效率提高。當然,過高的濃度并不能無限提高效率,反而會增加無謂的成本支出。當濃度大于500mg/L時,滅菌效率的提高已不明顯。然而,考慮到環(huán)氧乙烷氣體的損失,如水解和產(chǎn)品對氣體的吸收,實際選擇的濃度一般需高于理想作用濃度。
氣體滅菌并非迅速的滅菌方式,而需經(jīng)歷一段時間才能達到滅菌效果。以上各參數(shù)的選擇及產(chǎn)品、包裝、裝載形式等各因素的影響,都會導致所需滅菌時間的變化。
傳統(tǒng)無菌檢驗的局限性
傳統(tǒng)的監(jiān)測方法為無菌檢驗,即抽取滅菌后的產(chǎn)品在無菌實驗室中進行微生物培養(yǎng),觀察培養(yǎng)結(jié)果以確定該滅菌過程的有效性。然而,該種方式雖然能比較準確的反應(yīng)被檢測產(chǎn)品的帶菌情況,但其在環(huán)氧乙烷滅菌過程監(jiān)控方面的合理性和有效性存在以下的局限性。
無菌檢驗是一個抽檢過程,其有效性建立在其抽樣的合理性上。然而,由于環(huán)氧乙烷滅菌的影響因素很多、整個負載的均一性不高,無法找到可靠的抽樣方案以準確反映整個負載的滅菌效果。
另外,無菌檢驗還有結(jié)果等待周期長、投入設(shè)備和人力大、報廢產(chǎn)品成本高等缺點,從經(jīng)濟角度出發(fā),也不是滅菌質(zhì)量控制的理想方法。
生物監(jiān)測
要尋找適合的滅菌監(jiān)控手段,shou先需了解影響滅菌效果的主要因素。在滅菌環(huán)境相同的情況下,產(chǎn)品上負載的微生物的抗力和數(shù)量,是影響滅菌效率的關(guān)鍵因素。通常,由于對于原材料的來源和微生物的數(shù)量有嚴格要求,加上對于儲存和生產(chǎn)車間的潔凈要求(不同產(chǎn)品有不同要求),在滅菌前所攜帶的微生物的數(shù)量是有限的。生物監(jiān)測使用所攜帶微生物的數(shù)量和抗力都遠大于實際生物負載的生物指示劑,與生物負載處于相同或更難滅菌的環(huán)境中(如將生物指示劑放置于過程挑戰(zhàn)設(shè)備{Process Challenge Device}中) 同時進行滅菌,然后觀察生物指示劑中微生物的殺滅情況,來判斷整個負載的有效性。圖1解釋了生物指示劑監(jiān)控整個負載并可靠反映其效果的原理:當生物指示劑被殺滅的時候,生物負載早已被殺滅了。
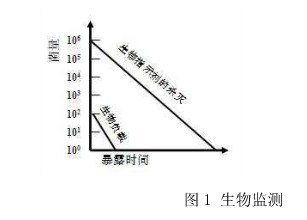
圖1 生物監(jiān)測
生物指示劑
當前用于滅菌效果驗證和監(jiān)測的生物指示劑,主要有菌片、自含式生物指示劑和芽孢懸浮液等幾種形式 。
菌片因其價格便宜而應(yīng)用廣泛。在滅菌結(jié)束后,將菌片轉(zhuǎn)移**配制好的培養(yǎng)基中進行培養(yǎng),培養(yǎng)**少7天后觀察微生物的生長情況,來判斷滅菌效果。
自含式生物指示劑,是將菌片和培養(yǎng)基集成在一個塑料小瓶中,在滅菌結(jié)束后,從瓶外捏破裝有培養(yǎng)基的玻璃安瓿,使培養(yǎng)液充分浸潤內(nèi)置的菌片,經(jīng)培養(yǎng)后觀察其變色情況或熒光反應(yīng)來判斷滅菌效果。
與菌片相比,自含式生物指示劑有以下優(yōu)點:
**,菌片滅菌后培養(yǎng)過程繁瑣,需經(jīng)歷配制培養(yǎng)基、培養(yǎng)基滅菌、無菌轉(zhuǎn)移和培養(yǎng)等一系列過程;而自含式生物指示劑,含內(nèi)置無菌培養(yǎng)液,操作簡便,大大簡化了操作人員的培訓過程。
第二,菌片無菌轉(zhuǎn)移過程中,如試樣被污染,則培養(yǎng)結(jié)果存在假陽性的可能。而假陽性是很難判斷的,因此一旦出現(xiàn)陽性,整批產(chǎn)品需重新進行滅菌,耗時耗力。而自含式生物指示劑采用密閉結(jié)構(gòu),其蓋中的過濾材料能透過環(huán)氧乙烷氣體和水蒸氣,可有效的阻隔微生物的侵入,避免假陽性的出現(xiàn)。
第三,菌片的培養(yǎng)時間較長,**少需要7天培養(yǎng)時間。而自含式生物指示劑只需2天,即能反映滅菌效果,能夠滿足市場對于企業(yè)日漸增強的快速供給的要求。
第四,通過顏色變化來判斷培養(yǎng)結(jié)果,相比通過混濁與否來觀察更明確、更容易判斷。
驗證和常規(guī)監(jiān)測
根據(jù)ISO11135規(guī)定,不能由隨后的產(chǎn)品檢驗和試驗來充分證實其結(jié)果的過程稱為特殊過程。滅菌過程就是這種特殊過程,通過前面的論述可知,包括無菌檢驗在內(nèi)的產(chǎn)品檢驗方法無法充分證明其結(jié)果——即無菌保證水平——的達到。對于這樣的工藝過程,必須進行預先的驗證和日常的監(jiān)控。
滅菌驗證,即是通過物理和生物實驗的方法,證明所設(shè)定的滅菌工藝過程及參數(shù),能夠保證產(chǎn)品滅菌工藝要求的達到。ISO11135規(guī)定, 驗證必須**少每年進行一次 。而且,一旦發(fā)生可能影響**終滅菌效果的改變——如更換包裝、改變裝載順序等——發(fā)生時,必須進行驗證。驗證的過程通常牽涉企業(yè)眾多部門,步驟繁多,耗時較長。簡要的驗證流程如下:
1) 驗證前準備
需要制定驗證方案,并由經(jīng)過培訓的人員來實施整個驗證。對于產(chǎn)品滅菌的適用性、包裝、滅菌劑、加濕蒸汽、生物指示劑等的適用性均需進行驗證并形成文件。
2) 安裝驗證
需要驗證的內(nèi)容包括設(shè)備的相關(guān)資料和附件是否齊全、安裝場所是否符合安全要求、對主要計量器具進行校驗等。計量器具的校驗必須shou先進行。
3) 運行驗證(試運行)
設(shè)備安裝后,應(yīng)按操作說明書啟動設(shè)備,確定設(shè)備是否能在預期的設(shè)計范圍內(nèi)準確的運行,并能達到各項技術(shù)指標和使用要求。
對于預處理區(qū),需驗證其空載狀態(tài)下的溫濕度均勻性;對于滅菌柜室,需驗證其空載狀態(tài)下的溫度均勻性。
4) 物理性能驗證
在滿載狀態(tài)下,驗證設(shè)備達到預期工藝參數(shù)的能力。對于預處理區(qū),需驗證其滿載狀態(tài)下的溫濕度均勻性;對于滅菌柜室,需驗證其滿載狀態(tài)下的溫度均勻性。
5) 微生物性能驗證
可以認為,之前的驗證目的在于確保設(shè)備主體及其他輔助用品能夠滿足工藝要求。而微生物性能驗證的目的在于,在這樣的條件下,尋找并證明能夠滿足滅菌工藝要求——10 -6 無菌保證水平——的工藝參數(shù)。
在選定的溫度、相對濕度和環(huán)氧乙烷濃度的條件下,能將生物指示劑的存活概率降低到10 -6 或以下的氣體作用時間,就是所需尋找的工藝參數(shù)。工業(yè)上,通常用半周期法來確定所需的滅菌時間。通過將滅菌時間依次減半,直**找到**短滅菌時間——即剛好能將生物指示劑殺滅的時間。用該時間重復兩次滅菌過程,需全部陰性。由于根據(jù)《ISO11138 醫(yī)療保健產(chǎn)品滅菌生物指示物》的規(guī)定,用于環(huán)氧乙烷滅菌驗證和監(jiān)測用的生物指示劑的**小菌量需達到1.0×10 6 ,該**短滅菌時間的兩倍,即為能滿足滅菌要求的氣體作用時間,如圖2所示。
需要提醒的是,半周期法雖然是**簡便的方法,卻并不是**可靠的。由于嚴格來講,對于生物指示劑的殺滅曲線是未知的,半周期法的結(jié)果只是建立在推測的基礎(chǔ)上。所以,有條件的企業(yè),應(yīng)該選用更嚴格、更可靠的存活曲線法或部分陰性法。
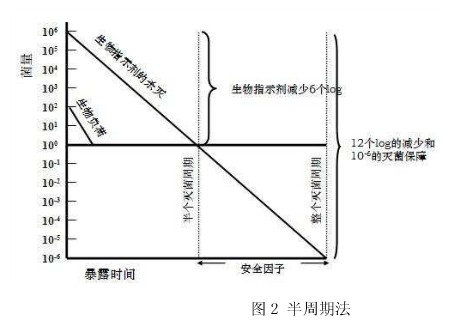
圖2 半周期法
驗證時生物指示劑需擺放在整個負載**難滅菌的部位,并應(yīng)達到一定的數(shù)量以全面反應(yīng)滅菌柜室內(nèi)各位置的滅菌效果。對于生物指示劑的擺放數(shù)量,ISO11135有如下的推薦:
☆ 柜室體積達到5m3 時,**少20支
☆ 柜室體積5 m3 -10m3 時,每增加1m3 ,增加2支
☆ 柜室體積>10m3 時,每增加2m3 ,增加2支
常規(guī)監(jiān)測用于對驗證后的日常滅菌過程進行監(jiān)測,控制產(chǎn)品放行。建議使用的生物指示劑的數(shù)量通常為驗證時的一半。
當前存在的問題
目前在G內(nèi),由于經(jīng)費的限制及認識的不足,對于工業(yè)上滅菌流程的規(guī)范,尚存在以下一些問題。
1) 驗證的不科學
“一招鮮”的驗證方法,在G內(nèi)還十分常見。所謂“一招鮮”,就是只對一種產(chǎn)品、一臺設(shè)備、一個裝載方式進行驗證,然后將這套滅菌工藝用于所有的產(chǎn)品、設(shè)備和裝載方式。
這主要是由于對驗證的認識不足導致的。驗證得到的滅菌參數(shù)只能用于該次驗證的滅菌工藝,因為不同的產(chǎn)品、設(shè)備、裝載等因素,都會對滅菌效果產(chǎn)生影響。對于不同的滅菌過程,沒有任何一套滅菌參數(shù)是可以確保滅菌效果的。必須對任何不同的滅菌過程分別的進行驗證,確定有科學依據(jù)的、可確保滅菌效果的滅菌參數(shù)。
另外,有很多企業(yè)未嚴格遵守ISO標準規(guī)定的驗證流程,文件系統(tǒng)的不規(guī)范、對于設(shè)備的驗證不充分等問題仍然存在。
2) 常規(guī)監(jiān)測的不重視
對于經(jīng)過驗證的滅菌過程,很多企業(yè)在日常的滅菌流程上,選擇了參數(shù)放行、化學監(jiān)測或無菌檢驗的方法來放行產(chǎn)品。以上這些控制方式,對于工業(yè)環(huán)氧乙烷滅菌來說,都是不充分的。
影響環(huán)氧乙烷滅菌效果的因素很多且相互關(guān)聯(lián),控制起來十分困難。
例如,濕度就是一個多變因素。即使經(jīng)過了有效的預處理,由于環(huán)境濕度的不穩(wěn)定、抽真空濕度損失等原因,滅菌作用過程中分散到每個包裹的濕度仍是不可預知和不可控制的。如使用混合環(huán)氧乙烷氣體,由于氣體的均勻性的不穩(wěn)定,實際作用在產(chǎn)品上的環(huán)氧乙烷濃度也是很難精確計算和控制的。另外,還有很多未知因素影響著環(huán)氧乙烷滅菌的有效性。因此,即使通過驗證確定了參數(shù),仍舊要對日常的滅菌進行常規(guī)監(jiān)測,確認滅菌實際有效后才能放行。
化學指示劑是通過滅菌過程對于化學物品的作用導致的化學變化,來模擬生物指示劑的滅活。然而,化學指示劑并不能代替生物指示劑的作用,**終能確定整個負載滅菌效果只有生物監(jiān)測。
3) 生物指示劑的選擇和用法不當
用作滅菌驗證和常規(guī)監(jiān)測的生物指示劑,需謹慎的選擇。性能符合ISO11138的規(guī)定并獲得上市許可,是選擇生物指示劑的基本條件。需要注意的是,如無菌產(chǎn)品將**終出口,所選擇的生物指示劑也需滿足該G的要求并獲得認可。
對于生物指示劑的使用,目前也存在著用量不足和用法不當?shù)葐栴}。
在滅菌柜室中使用足夠多的生物指示劑進行全面的監(jiān)測是必須的。然而,出于成本的考慮,一些企業(yè)未使用足夠多的生物指示劑進行驗證和常規(guī)監(jiān)測。其實,這樣所得的結(jié)果是不夠可靠的。因為無論是在驗證還是常規(guī)監(jiān)測時,只有全面監(jiān)控整個滅菌柜室的情況,才能使所得滅菌參數(shù)真正能夠保證滅菌的有效性。
另有一些企業(yè),在驗證和常規(guī)監(jiān)測時使用不同的生物指示劑或混用不同品牌的生物指示劑。由于不同的生物指示劑的菌量和抗力有所不同,這對于驗證和常規(guī)監(jiān)測的一致性是有影響的。
將生物指示劑放在**難滅菌部位,也是**關(guān)重要的。PCD為滅菌過程對生物指示劑的殺滅提供**大挑戰(zhàn),是保證生物監(jiān)測的有效性的重要手段。對PCD的可靠性,亦需進行驗證。
總結(jié)
由于環(huán)氧乙烷滅菌的過程復雜、導致其失敗的原因很多,并且沒有經(jīng)典的參數(shù)配置可以適用于各種情況,為了保證滅菌的質(zhì)量,對其進行嚴格的驗證和常規(guī)監(jiān)測是必要的。
生物監(jiān)測覆蓋了整個負荷,并能確實保證SAL的達到,是**能夠全面確保 滅菌效果 的監(jiān)測方式。
在高速發(fā)展的中G社會,對醫(yī)療服務(wù)與產(chǎn)品的質(zhì)量訴求不斷增高。對于日漸成熟的中G醫(yī)療產(chǎn)品企業(yè),更多的與G際接軌、與各G企業(yè)開展貿(mào)易的趨勢不可阻擋。無菌醫(yī)療產(chǎn)品的滅菌效果控制,是其質(zhì)量控制中的重中之重。不使用科學的、規(guī)范的手段確保滅菌效果的醫(yī)療產(chǎn)品,既很難滿足G內(nèi)市場日益增高的質(zhì)量訴求,也無法在G際市場上獲得認可。因此,規(guī)范滅菌工藝、確保滅菌質(zhì)量,成為無菌醫(yī)療產(chǎn)品生產(chǎn)企業(yè)的當務(wù)之急。